Antwort Was regelt die Medizinprodukteverordnung? Weitere Antworten – Was wird durch das Medizinproduktegesetz geregelt
Die neue Medizinprodukteverordnung (2017/745/EU) hat die Medizinprodukterichtlinie sowie die Richtlinie über aktive implantierbare medizinische Geräte ersetzt. Ziel ist die Sicherheit von Medizinprodukten über den gesamten Lebenszyklus weiter zu erhöhen.Januar 1995 in Kraft getreten ist. Das MPG regelt den Verkehr mit Medizinprodukten, insbesondere Inverkehrbringen und Inbetriebnahme dieser. Darüber hinaus regelt nun das MPDG ebenfalls den Anwendungsbereich.Medizinprodukte unterliegen u. a. der Verordnung (EU) 2017/745 über Medizinprodukte (MDR- Medical Device Regulation), und der Verordnung (EU) 2017/746 über In-vitro-Diagnostika (IVDR – In-vitro-Diagnostica Regulation), durchgeführt und ergänzt in nationales Recht durch das Medizinprodukterecht-Durchführungsgesetz (MPDG …
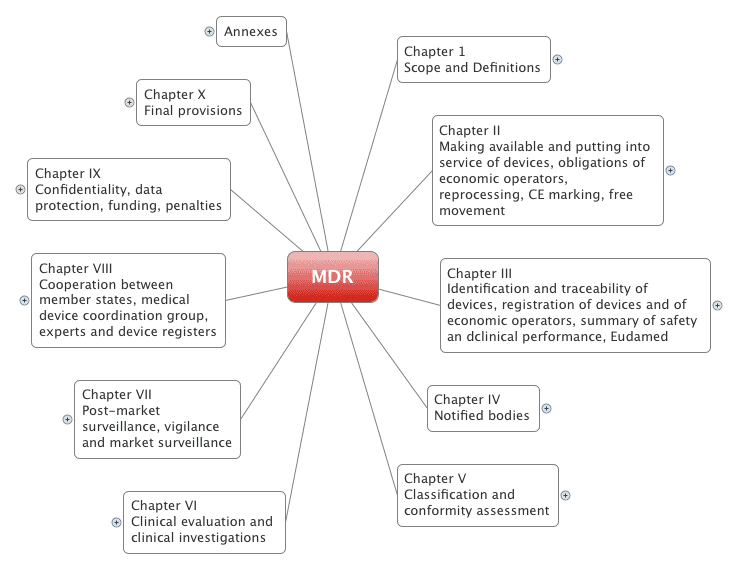
Was ist in der MDR geregelt : Die Medical Device Regulation (MDR) ist eine EU-Verordnung, die Hersteller einhalten müssen, die Medizinprodukte in der EU in den Verkehr bringen wollen. Sie betrifft auch Händler und Importeure dieser Produkte sowie Benannte Stellen.
Wer regelt das Medizinproduktegesetz
745/2017 (Medical Device Regulation). Diese Verordnung wurde vom Europäischen Parlament im Mai 2017 veröffentlicht und ist seit 26. Mai 2021 für alle Mitgliedstaaten und Hersteller verbindlich und unmittelbar anzuwenden.
Was löst die MDR ab : Die MDR löst die bisherigen Medizinprodukte-Richtlinien MDD (Richtlinie 93/42/EWG über Medizinprodukte) und AIMD (Richtlinie 90/385/EWG über aktive implantierbare Medizinprodukte) ab.
Am 26. Mai 2020 trat die MDR (Medical Device Regulation) in allen europäischen Ländern in Kraft. Diese Verordnung soll durch das MDG (Medizinprodukte-Durchführungsgesetz) in Deutschland ergänzt werden. Dadurch wird das bisherige MPG (Medizinproduktegesetz) abgelöst.
Das Medizinproduktegesetz (MPG) enthält die technischen, medizinischen und Informations-Anforderungen für das Inverkehrbringen von Medizinprodukten (durch Herstellung oder Einfuhr) im Europäischen Wirtschaftsraum (EWR).
Welche Anforderungen müssen Medizinprodukte erfüllen
3. Zulassung von Medizinprodukten in Europa
- Nachweis der grundlegenden Sicherheits- und Leistungsanforderungen in der Technischen Dokumentation.
- Nachweis des Nutzen-Risiko-Verhältnisses in der klinischen Bewertung.
- Post-Market-Surveillance.
- Vollständiges Qualitätsmanagementsystem des Herstellers.
1. Produkte, die unter den Anhang XVI fallen
| # | Beispiele |
|---|---|
| 1 | Farbige Kontaktlinsen |
| 2 | Subdermale Implantate wie Hornimplantate, Brustimplantate |
| 3 | Dermal Filler, z. B. Hyaluronspritzen |
| 4 | Bodyforming-Geräte, z. B. zur Fettabsaugung |
Mai 2021 in Kraft getreten ist. Das MPDG hat zu diesem Zeitpunkt das bisherige Medizinproduktegesetz ( MPG ) abgelöst, welches übergangsweise bis zum Geltungsbeginn der Verordnung ( EU ) 2017/746 nur noch für In-vitro-Diagnostika gilt.
Was ist die Medical Device Regulation Die Medical Device Regulation (MDR) regelt die Vorgaben, die Hersteller von Medizinprodukten einhalten müssen. Der deutsche Begriff dafür ist „Medizinprodukteverordnung“.
Welches Produkt ist kein Medizinprodukt : Software für allgemeine Zwecke hingegen, auch wenn sie im Gesundheitswesen eingesetzt wird, oder Software, die für die Lebensführung oder das Wohlbefinden bestimmt ist, gilt nicht als Medizinprodukt.
Was muss ein Medizinprodukt erfüllen : Medizinprodukte müssen für den Menschen bestimmt sein. Außerdem ist das Wirkprinzip wichtig. Medizinprodukte wirken im oder am menschlichen Körper (Ausnahme: Software), jedoch nicht pharmakologisch, metabolisch oder immunologisch. Die MDR gilt zudem für bestimmte Produkte ohne medizinischen Verwendungszweck, wie z.
Was definiert ein Medizinprodukt
Definition. Medizinprodukte sind Produkte mit medizinischer Zweckbestimmung, die vom Hersteller für die Anwendung beim Menschen bestimmt sind.
Nationale Gesetze
- Digitale-Versorgung-Gesetz ( DVG )
- Digitale-Versorgung-und-Pflege-Modernisierungs-Gesetz ( DVPMG )
Als Medizinprodukt werden unter anderem Apparate, Gegenstände, Stoffe und auch Software bezeichnet, die zu therapeutischen oder diagnostischen Zwecken für Menschen verwendet werden, wobei die bestimmungsgemäße Hauptwirkung im Unterschied zu Arzneimitteln primär nicht pharmakologisch, metabolisch oder immunologisch, …
Wie erkenne ich ein Medizinprodukt : Ein Medizinprodukt muss die vorgesehene CE-Kennzeichnung aufweisen. Ausnahmen von dieser Regel sind etwa Sonderanfertigungen, Produkte für klinische Prüfungen und Produkte mit Ausnahmegenehmigung. Um das CE-Zeichen zu erhalten, muss das Produkt die grundlegenden Anforderungen erfüllen.