Antwort Wie muss ein Medizinproduktebuch aussehen? Weitere Antworten – Was muss in einem Medizinproduktebuch stehen
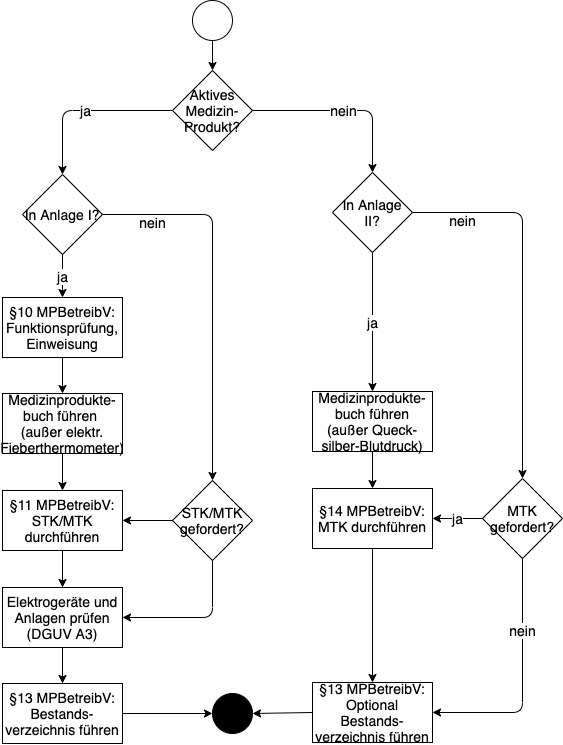
Im Medizinproduktebuch sind Angaben zur Identifikation eines Medizinproduktes, Belege für Funktionsprüfungen und Einweisungen, Fristen und Datum der Durchführung von sicherheitstechnischen Kontrollen, Datum Art und Folge von Funktionsstörungen sowie Angaben zu Vorkommnismeldungen enthalten.Zusätzlich zum Bestandsverzeichnis muss das Medizinproduktebuch für Medizinprodukte der Anlage 1 und Anlage 2 MPBetreibV geführt werden. Dazu zählen z. B. Defibrillatoren, Reizstromtherapiegeräte, HF-Chirurgiegeräte, Infusionsgeräte, Blutdruckmessgeräte, Ergometer, Thermometer oder Augentonometer.Mindestens alle zwei Jahre die Durchführung von sicherheitstechnischen Kontrollen STK (§ 11 MPBetreibV) (s. u.) Führen eines Medizinproduktebuchs (§ 12 MPBetreibV) und Bestandsverzeichnisses (§ 13 MPBetreibV) Messtechnische Kontrollen MTK (§ 14 MPBetreibV) (s. u.)
Welche Medizinprodukte müssen ins Bestandsverzeichnis : Die aktiven Medizinprodukte (aktives Medizinprodukt = energetisch betriebenes Medizinprodukt. Energiequellen können z.B. Strom [Netz, Akku, Batterie] oder Druckluft sein) müssen in einer Bestandsliste geführt werden. Die Liste kann sowohl in Papierform als auch per EDV geführt werden (bei EDV Datensicherung beachten).
Welche Medizinprodukte müssen in das Medizinproduktebuch eingetragen werden
Im Medizinproduktebuch finden sich detaillierte Angaben zu den einzelnen im Betrieb verwendeten Medizinprodukten. Dazu gehören u.a.: Angaben zur Geräteidentifikation: Gerätestammdaten, Zubehör, Prüfintervalle. Belege über Funktionsprüfungen und Einweisungen.
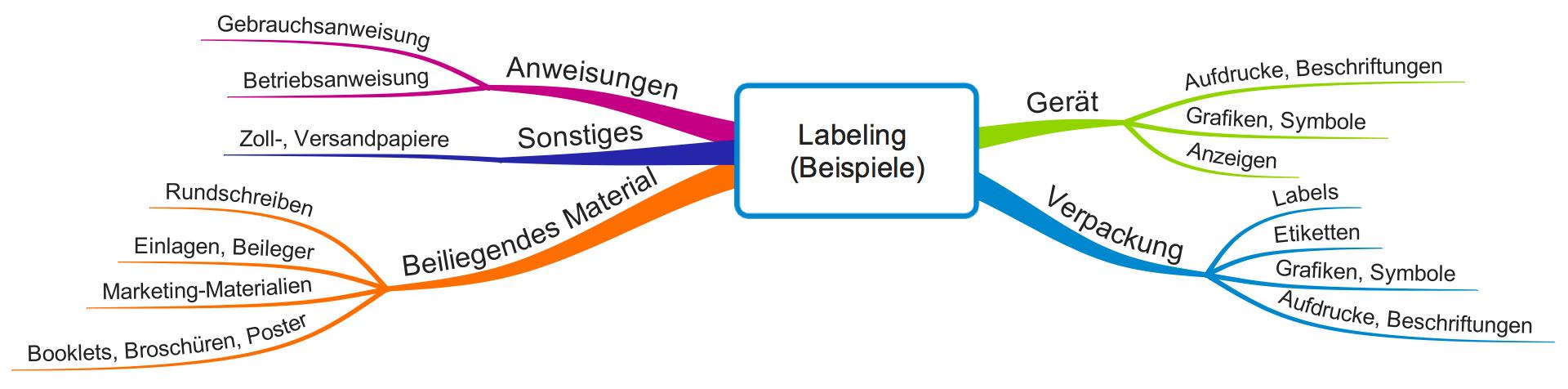
Welche Dokumente sind für ein Medizinprodukt gemäß MDR erforderlich : Alle Medizinprodukte müssen eine eindeutige Identifizierung erhalten, die UDI. Damit müssen die Produkte in der EUDAMED registriert werden. Die MDR legt Anforderungen an die Gebrauchsanweisung, weitere Begleitmaterialien und das sonstige Labeling wie Aufdrucke und Verpackungen genau fest.
Blutdruckmessgeräte oder andere aktive Medizinprodukte, die als Vorführgeräte in der Apotheke ausgestellt werden, müssen als solche deklariert werden und müssen die MDR nicht erfüllen.
Zu den nichtaktiven Medizinprodukten zählen beispielsweise Implantate, chirurgische Instrumente, Gehilfen, Verbandsmaterial, Kondome usw.
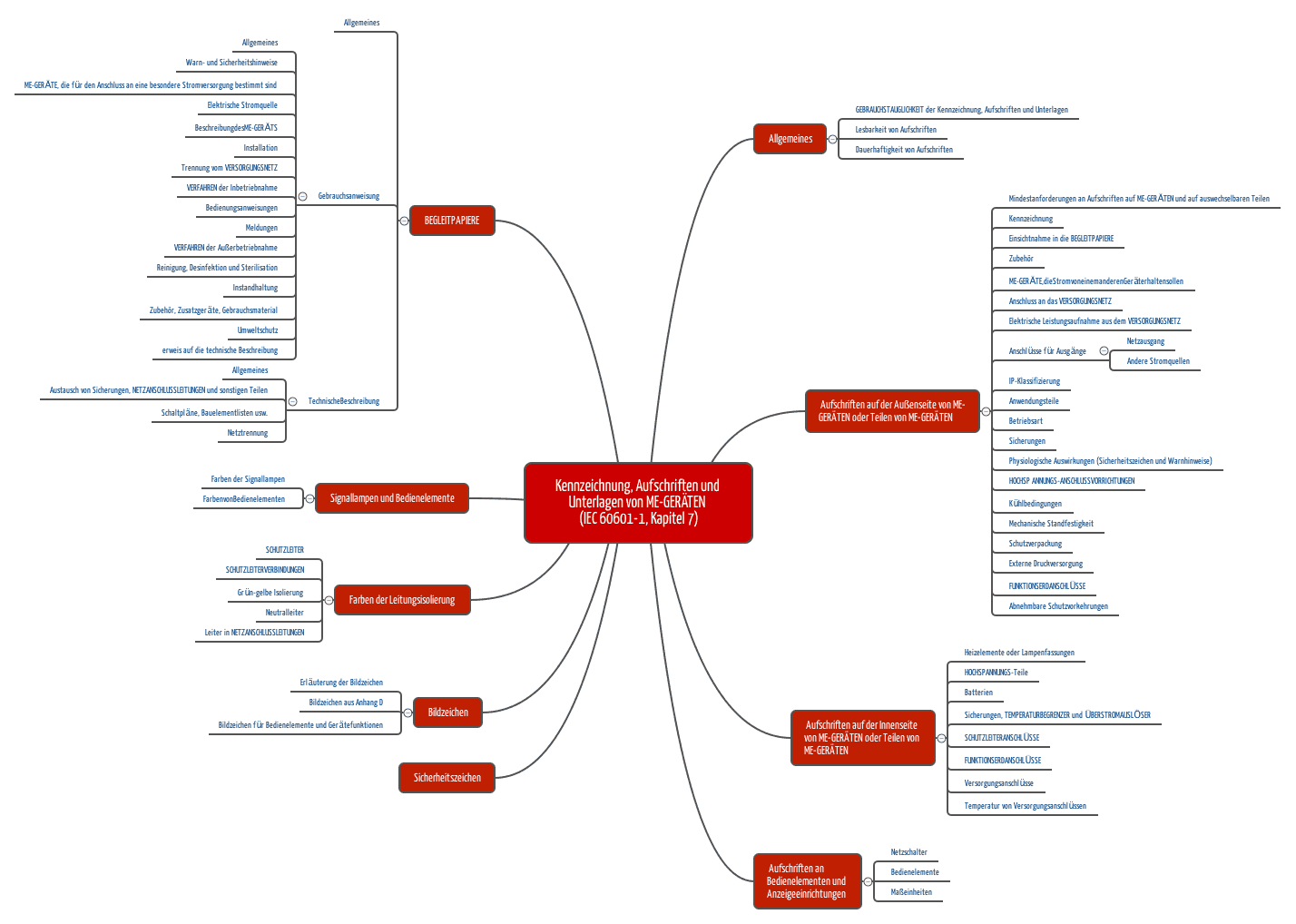
Wie muss ein Medizinprodukt gekennzeichnet sein
Medizinprodukte dürfen in Deutschland und der EU nur in Verkehr gebracht und auf dem Markt bereitgestellt oder in Betrieb genommen werden, wenn sie mit einer CE-Kennzeichnung versehen sind. Der CE-Kennzeichnung folgt, wo erforderlich, die vierstellige Kennnummer einer sog. Benannten Stelle.Um ein Medizinprodukt zuzulassen, muss der Hersteller umfangreiche Dokumentation und klinische Daten vorlegen, die zeigen, dass das Produkt sicher und wirksam ist. Diese Daten werden von der zuständigen Behörde geprüft, um sicherzustellen, dass das Produkt den Anforderungen entspricht.Medizinprodukte sind Produkte mit medizinischer Zweckbestimmung, die vom Hersteller für die Anwendung beim Menschen bestimmt sind und primär physikalisch wirken ( z.B. Implantate, Herzschrittmacher, etc. ). Sie werden entsprechend ihrer Risikoklasse (I- III , gering bis sehr hoch) eingestuft und geprüft.
3. Zulassung von Medizinprodukten in Europa
- Nachweis der grundlegenden Sicherheits- und Leistungsanforderungen in der Technischen Dokumentation.
- Nachweis des Nutzen-Risiko-Verhältnisses in der klinischen Bewertung.
- Post-Market-Surveillance.
- Vollständiges Qualitätsmanagementsystem des Herstellers.
Welche 2 Gesetze regeln die Grundlagen in Bezug auf Medizinprodukte : Medizinprodukterecht-Durchführungsgesetz
Seit dem 26. Mai 2021 lösen die MDR und das MPDG das Medizinproduktegesetz ( MPG ) für alle Produkte im Anwendungsbereich der MDR ab.
Welches Produkt ist kein Medizinprodukt : Software für allgemeine Zwecke hingegen, auch wenn sie im Gesundheitswesen eingesetzt wird, oder Software, die für die Lebensführung oder das Wohlbefinden bestimmt ist, gilt nicht als Medizinprodukt.
Wie erkenne ich ein Medizinprodukt
Ein Medizinprodukt muss die vorgesehene CE-Kennzeichnung aufweisen. Ausnahmen von dieser Regel sind etwa Sonderanfertigungen, Produkte für klinische Prüfungen und Produkte mit Ausnahmegenehmigung. Um das CE-Zeichen zu erhalten, muss das Produkt die grundlegenden Anforderungen erfüllen.
Mai 2021 in Kraft getreten ist. Das MPDG hat zu diesem Zeitpunkt das bisherige Medizinproduktegesetz ( MPG ) abgelöst, welches übergangsweise bis zum Geltungsbeginn der Verordnung ( EU ) 2017/746 nur noch für In-vitro-Diagnostika gilt.Medizinprodukte sind Produkte mit medizinischer Zweckbestimmung, die vom Hersteller für die Anwendung beim Menschen bestimmt sind.
Was zählt nicht zu Medizinprodukten : Beispiele für Produkte, die nicht als Medizinprodukte zählen
Krankenhaus-Informationssysteme, die nur der Dokumentation dienen. Die meisten Wellness- und Fitness-Produkte. Arzneimittel. Produkte, die vom Hersteller nicht speziell für die Anwendung am Patienten in den Markt gebracht wurden, aber dafür genutzt werden …